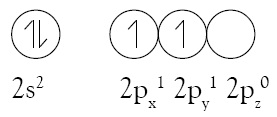- berikatan kovalen tunggal yang jenuh;
- berikatan kovalen tunggal yang tidak jenuh (memiliki elektron bebas); dan
- berikatan kovalen rangkap.
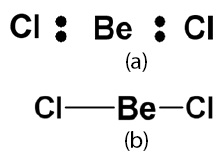 |
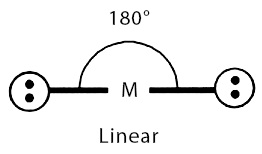
| Gambar 1. (a) Struktur Lewis BeCl2 (b) Bentuk molekul BeCl2 (linear) |
 |
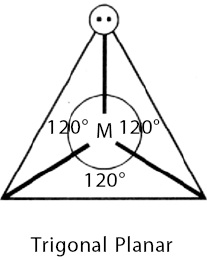
| Gambar 2. (a) Struktur Lewis BeCl3 (b) Bentuk molekul BeCl3 (trigonal planar). |

 |
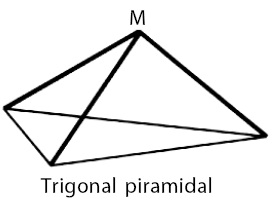
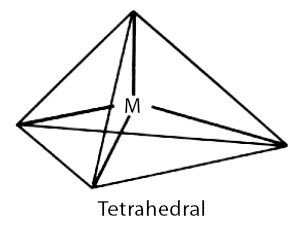
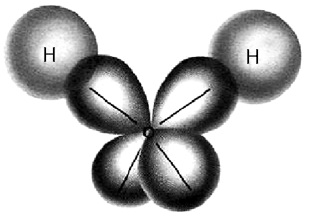
| Gambar 3. (a) Struktur Lewis NH3 (b) Bentuk molekul NH3 (trigonal piramidal) (c) Struktur ruang pasangan elektron dalam kulit valensi atom N (tetrahedral) |

Bagaimanakah pandangan teori domain elektron terhadap molekul yang memiliki ikatan kovalen rangkap dua atau rangkap tiga? Menurut teori domain elektron, ikatan rangkap dianggap sebagai satuan gugus elektron seperti halnya ikatan tunggal yang menghubungkan atom dengan atom pusat M. Contohnya, molekul CO2 yang mengandung ikatan rangkap dua. Menurut teori domain elektron, bentuk molekul CO2 dapat dianggap sebagai dua gugus pasangan elektron ikatan, seperti pada molekul BeCl2. Oleh karena itu, bentuk molekul CO2 dianggap linear (perhatikan Gambar 4a).
 |
| Gambar 4. (a) Struktur Lewis dan bentuk molekul CO2 (b) Struktur Lewis dan bentuk molekul HCN. |
Contoh Soal 3 (Meramalkan Geometri Molekul Berikatan Rangkap) :
| Pasangan Elektron | Struktur
Ruang Pasangan Elektron |
Bentuk Molekul | Kelompok | Contoh
Molekul |
||
| Total | Ikatan | Bebas | ||||
| 2 | 2 | 0 | Linear | Linear | MX2 | BeCl2 |
| 3 | 3 2 | 0 1 | Trigonal planar | Trigonal planar
Huruf |
MX3
MX2E |
BH3 dan BCl
SnCl2 |
| 4 | 4 3 2 | 0 1 2 | Tetrahedral | Tetrahedral
Trigonal piramidal Huruf |
MX4
MX3E MX2E2 |
CCl4 dan SiH
NH3 dan PCl H2O dan SCl |
| 5 | 5 4 3 2 | 0 1 2 3 | Trigonal bipiramidal | Trigonal bipiramidal
Disfenoidal Bentuk–T Linear |
MX5
MX4E MX3E2 MX2E3 |
PCl5 dan PF5
SF4 ClF3 XeF2 |
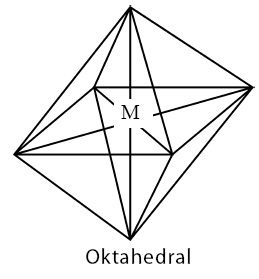
| 6 | 6 5 4 | 0 1 2 | Oktahedral | Oktahedral
Piramida alas bujur sangkar Bujur sangkar |
MX6
MX5E MX4E2 |
SF6
ClF5 XeF4 |
- Ketika membentuk ikatan, orbital-orbital pada atom pusat mengadakan restrukturisasi melalui proses hibridisasi membentuk orbital hibrida. Selanjutnya, orbital hibrida ini berikatan dengan orbital atom lain.
- Orbital-orbital yang berikatan harus bertumpang tindih (overlapping) satu sama lain.
- Jumlah elektron dalam orbital ikatan yang bertumpang tindih maksimal dua elektron dengan spin berlawanan.
- Kekuatan ikatan bergantung pada derajat tumpang tindih. Semakin besar daerah tumpang tindih, semakin kuat ikatan yang terbentuk.
- Orbital-orbital atom selain orbital-s dalam berikatan memiliki arah tertentu sesuai orientasi orbital atom yang berikatan.
Kedua orbital yang berikatan (1s-sp3) dilokalisasikan sepanjang ikatan C–H. Oleh karena itu, orbital yang terbentuk dinamakan orbital ikatan terlokalisasi yang diorientasikan pada daerah di antara atom karbon dan hidrogen.Model orbital ikatan terlokalisasi merupakan aplikasi teori ikatan valensi yang dikembangkan oleh Linus Pauling.
Apakah yang dimaksud dengan hibridisasi? Hibridisasi adalah proses pencampuran orbital-orbital atom membentuk orbital baru dengan tingkat energi berada di antara orbital-orbital yang dicampurkan. Orbital hasil pencampuran dinamakan orbital hibrida.Mengapa orbital-orbital berhibridisasi? Untuk dapat menjawab hal ini, tinjau molekul CH4 yang dibentuk dari satu atom karbon dan empat atom hidrogen dihubungkan dengan konfigurasi elektron atom karbon.
Jika Anda perhatikan konfigurasi elektron valensi tersebut, atom karbon hanya memiliki 2 elektron yang tidak berpasangan. Seharusnya, atom karbon maksimal mengikat 2 atom hidrogen membentuk CH2, seperti pada molekul PCl3 (Gambar 8). Perhatikan Gambar 7.
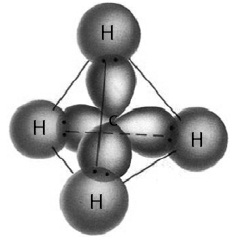 |
| Gambar 7. Orbital sp3 dari atom C bertumpang tindih dengan orbital s dari atom H. |
Mengapa atom karbon dapat membentuk empat ikatan kovalen dengan atom-atom lain? Kasus ini dan untuk semua molekul yang lain dapat dijelaskan dengan pendekatan hibridisasi.
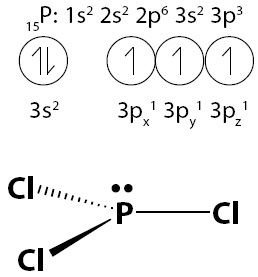 |
| Gambar 7. Pada PCl3, elektron dari setiap atom Cl berikatan dengan elektron dari atom P membentuk 3 pasang elektron ikatan. |
Simak kembali molekul CH4. Ketika atom hidrogen mendekati atom karbon, terjadi perubahan tingkat energi orbital-orbital pada atom karbon sedemikian rupa sehingga dimungkinkan terjadinya hibridisasi orbital-orbital valensi atom karbon.
Oleh karena orbital-orbital hibrida yang dibentuk memiliki tingkat energi yang sama (di antara 2s dan 2p) maka elektron yang berasal dari orbital 2s dipromosikan ke orbital p3 yang masih kosong. Orbital hibrida tersebut dinamakan orbital sp3 karena berasal dari satu orbital-s dan tiga orbital-p.
Berdasarkan tabel berikut :
| Senyawa | Mr | Titik Didih |
| NH3 | 17 | –33 |
| PH3 | 34 | –88 |
| AsH3 | 78 | –55 |
| SbH3 | 125 | –17 |
Molekul PH3 memiliki titik didih terendah penyebabnya adalah ….
- Mr terkecil
- Molekulnya kecil
- Terdapatnya ikatan hidrogen
- Terdapatnya ikatan gaya London
- Terdapatnya ikatan gaya Van der Waals
Pembahasan :
Pada molekul PH3, terdapat gaya Van der Waals. Ikatan Van der Waals jauh lebih lemah daripada ikatan hidrogen pada molekul NH3. Karenanya PH3 memiliki titik didih terendah (E)
Pembentukan orbital hibrida sp dapat ditunjukkan pada gambar berikut.
 |
| Gambar 9. Pembentukan orbital hibrida sp. Hibridisasi orbital atom s dan orbital atom p menghasilkan orbital hibrida sp dengan orientasi ruang membentuk sudut 180°. |
- Setiap orbital menyediakan daerah tumpang tindih yang cukup besar dengan orbital 1s dari atom hidrogen.
- Orbital-orbital tersebut memiliki orientasi 180° satu sama lain.
Agar atom B dapat berikatan dengan tiga atom F maka orbital-orbital 2s pada kulit valensi mengadakan hibridisasi dengan orbital 2p, diikuti promosi elektron dari orbital 2s ke orbital 2p. Hasilnya adalah sebagai berikut.
 |
| Gambar 14. Empat orbital ikatan terlokalisasi dalam CH4 dibentuk melalui tumpang tindih orbital hibrida sp3 pada atom C dan 1s dari atom H. |
Tinjau molekul PCl5 dengan atom P sebagai atom pusat. Konfigurasi elektronnya: 15P : 1s2 2s2 2p6 3s2 3p33d0. Hibridisasi satu orbital 3s, tiga orbital 3p dan satu orbital 3d menghasilkan lima orbital hibrida sp3d dengan struktur trigonal bipiramidal yang simetris. Kelima orbital hibrida sp3d memiliki sifat-sifat menarik sebab ada dua orbital hibrida yang tidak setara.
Keenam orbital sp3d2 bertumpang tindih dengan orbital 2p dari atom fluorin membentuk enam ikatan S–F terlokalisasi yang setara dengan struktur oktahedral.
Apakah hibridisasi terjadi pada senyawa karbon, khususnya ikatan pada karbon-karbon? Tinjau molekul etana (C2H6) dengan struktur molekul ditunjukkan berikut.
 |
| Gambar 16. (a) Struktur molekul etana (b) Struktur orbital pada molekul etana. |
Bentuk molekul etana dapat dijelaskan dengan orbital hibrida sp3 pada kedua atom karbon. Ikatan C–C dibentuk melalui tumpang tindih antara orbital sp3 dan orbital sp3 dari masing-masing atom karbon. Enam ikatan C–H dibentuk melalui tumpang tindih orbital sp3 sisa dan orbital 1s dari atom H. Struktur orbital pada molekul etana ditunjukkan pada Gambar16b.
 |
| Gambar 19. Kerangka ikatan dalam asetilen. Orbital ikatan C–C hasil dari tumpang tindih dua orbital hibrida sp. Dua orbital ikatan C–H hasil dari tumpang tindih orbital sp dan 1s dari hidrogen. |
Terdapat sejumlah molekul yang memiliki ikatan π (phi). Salah satu contoh yang penting adalah molekul benzena (C6H6). Molekul benzena secara prinsip memiliki dua bentuk resonansi yang dapat diungkapkan dalam bentuk hibrida resonansi, yaitu:
Orbital hibrida sp2 yang pertama digunakan berikatan dengan orbital 1s dari atom hidrogen. Dua orbital hibrida sp2 yang lain digunakan untuk berikatan dengan orbital sp2 dari atom-atom karbon yang berdampingan. Semua ikatan yang dibentuk adalah ikatan sigma, seperti ditunjukkan pada Gambar 20.
 |
| Gambar 20. Tumpang tindih orbital hibrida sp2– sp2 dalam molekul benzena membentuk ikatan sigma. |
Setiap atom karbon memiliki orbital 2p sisa yang tegak lurus terhadap bidang heksagonal, seperti ditunjukkan pada Gambar 21.
 |
| Gambar 21. Tumpang tindih orbital 2p yang tidak digunakan dalam hibridisasi membentuk ikatan phi (Ikatan phi dalam benzena menjadikan elektron-elektron terdelokalisasi dalam molekul benzena). |
Keenam orbital 2p tersebut bertumpang tindih membentuk tiga ikatan pi. Ikatan pi ini tidak diasosiasikan dengan setiap pasang atom karbon tertentu melainkan orbitalorbital tersebut membentuk orbital terdelokalisasi.
Kekuatan gaya antar molekul lebih lemah dibandingkan ikatan kovalen maupun ikatan ion. Ikatan kimia dan gaya antarmolekul memiliki perbedaan. Ikatan kimia merupakan gaya tarik menarik di antara atom-atom yang berikatan, sedangkan gaya antar molekul merupakan gaya tarik menarik di antara molekul (perhatikan Gambar 22).
 |
| Gambar 22. Gaya antar molekul adalah gaya yang lebih lemah dibandingkan ikatan kimia. |
Pada antaraksi dipol-dipol, ujung-ujung parsial positif suatu molekul mengadakan tarikan dengan ujung-ujung parsial negatif dari molekul lain yang mengakibatkan orientasi molekul-molekul sejajar, seperti ditunjukkan pada Gambar 23.
 |
| Gambar 23. Gaya dipol-dipol permanen. |
Tabel 2. menunjukkan perbandingan sifat-sifat senyawa untuk massa molekul yang relatif sama dengan berbagai gaya antarmolekul.
Tabel 2. Sifat Fisika Molekul Hidrida Periode ke-4
| Sifat-Sifat Fisika | SiH4 | PH3 | H2S |
| Kepolaran | Nonpolar | Polar | Polar |
| Wujud | Gas | Gas | Gas |
| Massa molekul | 32,09 | 34,0 | 34,08 |
| Titik leleh (°C) | –185 | –134 | –85,6 |
| Titik didih (°C) | –111 | –87,8 | –60,8 |
| Kalor lebur (kJ mol–1) | 0,66 | 1,13 | 2,38 |
| Kalor uap (kJ mol–1) | 13 | 14,6 | 18,7 |
| Momen dipol | 0 | 0,55 | 1,10 |
| Sumber: Chemistry with Inorganic Qualitative Analysis, 1989 | |||
Simak sifat-sifat fisika SiH4, PH3, dan H2S pada Tabel 2. tersebut. Senyawa-senyawa tersebut memiliki massa molekul relatif yang sama. Molekul SiH4 bersifat nonpolar, memiliki titik leleh dan titik didih paling tinggi serta kalor peleburan dan kalor penguapan juga rendah. Molekul H2S memiliki momen dipol dua kali dari PH3 dan sesuai ramalan bahwa sifat-sifat fisika H2S lebih tinggi PH3 dan SiH4.
Gaya London adalah gaya yang terjadi pada atom atau molekul, baik polar maupun nonpolar. Gaya London atau disebut juga gaya dispersi, yaitu gaya yang timbul akibat dari pergeseran sementara (dipol sementara) muatan elektron dalam molekul homogen. Dalam ungkapan lain, dapat dikatakan bahwa gaya London terjadi akibat kebolehpolaran atau distorsi “awan elektron” dari suatu molekul membentuk dipol sementara (molekul polar bersifat dipol permanen).
- Pada sekumpulan besar molekul, setiap saat selalu terjadi tumbukan antar molekul, tumbukan ini menimbulkan dipol sementara membentuk muatan parsial positif pada salah satu ujung molekul dan muatan parsial negatif pada ujung yang lain (terdistorsi).
- Molekul-molekul yang terdistorsi selanjutnya menginduksi molekul lain membentuk dipol terinduksi.
- Akibat terbentuk dipol sementara pada sejumlah molekul yang bertumbukan dan menginduksi sejumlah molekul lain membentuk dipol terinduksi, menimbulkan gaya tarik-menarik di antara molekul-molekul tersebut. Gaya tarik-menarik seperti ini dinamakan gaya London.
- Gejala tersebut berlangsung secara terus menerus dan berimbas kepada molekul-molekul lain sehingga terjadi gaya London di antara molekul-molekul yang ada.
Tabel 3. Titik Didih Beberapa Senyawa Nonpolar
| Keadaan | Nama Senyawa | Rumus Struktur | Titik Didih
(°C) |
| Massa molekul
sama, bentuk molekul yang sperik (bulat) menurun |
Neopentana | 9,5 | |
| Isopentana | 28 | ||
| n–pentana | CH3CH2CH2CH2CH3 | 36 | |
| Bentuk molekul
serupa, massa molekul meningkat |
Metana | CH4 | –161 |
| Etana | CH3CH3 | –88,6 | |
| n–propana | CH3CH2CH3 | –44,5 | |
| n–butana | CH3CH2CH2CH3 | –0,5 | |
| Sumber: Chemistry with Inorganic Qualitative Analysis, 1989 | |||
Apakah yang dapat Anda simpulkan dari data tersebut? Perhatikan tingkat speritas molekul. Oleh karena neopentana lebih sperik dari molekul yang lain maka bidang sentuhnya paling kecil sehingga peluang terciptanya gaya London relatif kecil. Akibatnya, gaya tarik antarmolekul lemah. Hal ini ditunjukkan oleh titik didih yang relatif rendah.
Di antara bentuk molekul yang serupa, gaya London meningkat dengan bertambahnya jumlah elektron atau dengan bertambahnya massa molekul. Butana memiliki jumlah elektron lebih rumit dibandingkan molekul lain sehingga gaya Londonnya lebih besar. Ini ditunjukkan oleh titik didihnya yang paling tinggi.
Jika hanya antaraksi akibat kepolaran maka molekul H2S dan H2O memiliki sifat fisik yang relatif sama sebab keduanya polar. Akan tetapi, fakta menunjukkan bahwa pada suhu kamar, H2O berwujud cair dan H2S berwujud gas. Apa yang salah dengan konsep kepolaran? Konsep kepolaran tidak salah, tetapi ada faktor lain selain kepolaran. Berdasarkan hasil pengamatan, dalam senyawa-senyawa polar yang mengandung atom hidrogen ada antaraksi yang lebih kuat dibandingkan antaraksi dipol maupun gaya London. Antaraksi ini dinamakan ikatan hidrogen (perhatikan Gambar 24).
 |
| Gambar 24. Ikatan hidrogen pada air. |
Tabel 4 Sifat Fisik Senyawa Hidrida Non logam
| Sifat-Sifat | NH3 | PH3 | H2O | H2S | HF | HCl |
| Kepolaran | Polar | Polar | Polar | Polar | Polar | Polar |
| Wujud | Gas | Gas | Cair | Gas | Asap | Gas |
| Massa molekul | 17,03 | 34,0 | 18,02 | 34,08 | 20,01 | 36,46 |
| Titik leleh°C | –78 | –134 | 0,0 | –85,6 | –83,0 | –114 |
| Titik didih°C | –33 | –87,8 | 100,0 | –60,8 | 19,5 | –84,9 |
| Kalor lebur(kJ mol–1) | 5,52 | 1,13 | 6,02 | 2,38 | 4,56 | 1,99 |
| Kalor uap(kJ mol–1) | 23,3 | 14,6 | 40,7 | 18,7 | 25,6 | 16,1 |
Tabel 4. menunjukkan sifat-sifat fisik senyawa hidrida periode ke- 2 dan periode ke-3 dalam tabel periodik. Periode ke-2, yaitu NH3, H2O, dan HF, sedangkan periode ke-3, yaitu PH3, H2S, dan HCl. Pasangan seperti NH3–PH3; H2O–H2S; dan HF–HCl berasal dari golongan yang sama dalam tabel periodik. Dari pasangan tersebut, NH3, H2O, dan HF memiliki massa molekul lebih kecil, tetapi memiliki titik leleh dan titik didih lebih tinggi dibandingkan senyawa yang segolongan (lihat grafik pada Gambar 25).
 |
| Gambar 26. (a) Ikatan hidrogen dapat berupa ikatan antarmolekul (b) Ikatan hidrogen dalam molekul. |
Ikatan hidrogen antarmolekul adalah ikatan antara dua atau lebih molekul, baik molekul yang sama maupun molekul berbeda. Misalnya, antarmolekul H2O, NH3, CH3CH2OH, HF, atau SiF4. Ikatan hidrogen dalam molekul adalah ikatan antara dua gugus atom dalam suatu molekul, misalnya dalam asam benzoat.
Ikatan Hidrogen pada DNA
DNA, pembawa informasi genetika (memungkinkan informasi genetika terwariskan) adalah molekul yang berukuran sangat besar, terdiri atas dua utas rantai yang saling berhadapan membentuk rantai ganda berpilin. Rantai ganda berpilin ini terbentuk karena adanya ikatan hidrogen antara kedua utas rantai penyusun DNA. Oleh karena kekuatan ikatan hidrogen lebih kecil dari ikatan kovalen atom-atom penyusun rantai maka kedua utas rantai DNA dapat dipisahkan dan mengalami replikasi (penggandaan DNA).
Contoh Soal Gaya Antar Molekul :
d. CH3OH
- Bentuk molekul ditentukan oleh jumlah ikatan setiap atom dan sudut ikatan di antara atom-atom.
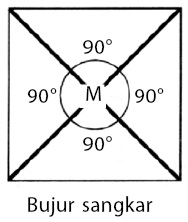
- Ada tujuh macam bentuk dasar molekul, yaitu linear, trigonal planar, bujur sangkar, tetrahedral, limas segitiga, trigonal bipiramidal, dan oktahedral.
- Teori domain elektron dapat dipakai untuk meramalkan bentuk molekul berdasarkan pada tolakan antara pasangan elektron dalam kulit valensi atom pusat.
- Jika dalam atom pusat terdapat pasangan elektron bebas sebanyak satu atau lebih, bentuk molekul yang dihasilkan dapat berubah dari bentuk dasarnya sebab pasangan elektron bebas memiliki kekuatan tolakan lebih kuat pasangan elektron lain .
- Urutan kekuatan tolakan di antara pasangan elektron, yaitu PEB–PEB > PEB–PEI > PEI–PEI
- Teori ikatan valensi dapat digunakan untuk mengevaluasi bentuk molekul berdasarkan pendekatan hibridisasi orbital atom.
- Hibridisasi adalah pencampuran (kombinasi) orbital-orbital atom membentuk orbital hibrida dengan tingkat energi berada di antara orbital-orbital atom yang dihibridisasikannya.
- Jenis hibridisasi pada kulit valensi atom pusat dapat ditentukan dari bentuk molekul. Hibridisasi sp terjadi pada molekul linear, sp2 pada molekul trigonal planar, sp3 pada molekul tetrahedral, dsp3 pada molekul dwilimas segitiga, dan d2sp3 pada molekul tetrahedral.
- Ikatan yang terjadi di antara orbital hibrida dengan orbital atom maupun orbital hibrida yang lain dinamakan ikatan sigma. Orbital atom yang tidak digunakan dalam hibridisasi jika digunakan untuk berikatan akan membentuk ikatan pi.
- Wujud suatu materi, seperti gas, cair, dan padat ditentukan oleh gaya antar molekul. Ada tiga jenis gaya, yaitu gaya dipol-dipol, gaya London, dan ikatan hidrogen. Gaya dipol-dipol dan gaya London tergolong gaya van der Waals.
- Gaya dipol-dipol adalah antar aksi antara molekul-molekul yang memiliki kepolaran. Kepolaran dalam molekul terjadi akibat perbedaan skala keelektronegatifan atom yang membentuk molekul.
- Gaya dispersi London yang disebabkan oleh adanya dipol sementara sebagai akibat tumbukan antaratom atau molekul yang berdekatan.
- Gaya dipol yang lebih kuat terjadi pada molekul yang mengandung atom hidrogen terikat pada unsur dengan keelektronegatifan tinggi, seperti nitrogen, oksigen, atau fluorin. Gaya dipol yang dihasilkan dinamakan ikatan hidrogen.
Referensi :
Sunarya, Y. dan A. Setiabudi. 2009. Mudah dan Aktif Belajar Kimia 2 : Untuk Kelas XI Sekolah Menengah Atas/Madrasah Aliyah Program Ilmu Pengetahuan Alam. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta. p. 250.